

La Diagnosi Genetica Preimpianto (DGP) permette di identificare e prevenire la trasmissione alla prole di malattie gravi causate da alterazioni genetiche e cromosomiche negli embrioni prima di trasferirli nell’utero, evitando così che nascano bambini affetti da malattie ereditarie.


Il Test Genetico Preimpianto (PGT, per la sua sigla in inglese) viene effettuato presso i Centri IVI autorizzati e rileva alterazioni genetiche e cromosomiche negli embrioni prima del transfer in utero. In questo modo è possibile prevenire la trasmissione alla prole di malattie ereditarie gravi, oltre ad evitare di trasferire embrioni che non genererebbero gravidanza. Esistono tre varianti del PGT, a seconda dell’alterazione che si dovrà rilevare.
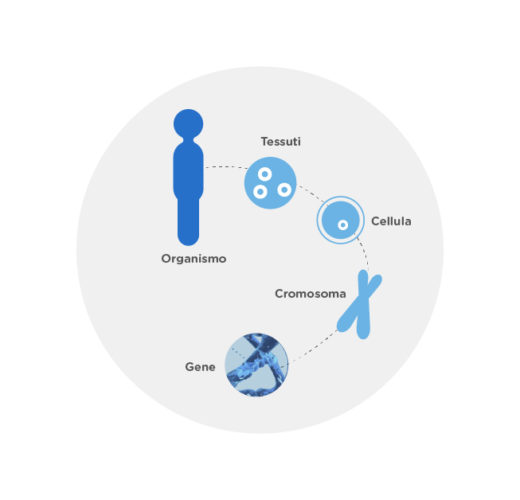
I cromosomi sono strutture che si trovano all’interno di ogni cellula e contengono informazioni genetiche, il nostro DNA. I geni, a loro volta, sono segmenti del DNA che contengono le informazioni sul funzionamento dell’organismo. L’essere umano presenta 23 paia di cromosomi: 22 autosomi e un paio di cromosomi sessuali (XX nel caso delle donne e XY nel caso degli uomini). Con la fecondazione dell’ovulo con lo spermatozoo, ogni genitore apporta un cromosoma di ogni paio, e trasmette la propria eredità.
Tuttavia, in alcune occasioni si verificano dei cambiamenti che possono generare alterazioni cromosomiche. Ne esistono di due tipi: numeriche – quando ci sono cromosomi in più o in meno – e strutturali –quando manca o eccede un frammento di un cromosoma specifico o è spostato su un altro cromosoma o è invertito.
Altre volte, l’alterazione avviene in un gene specifico e ciò influisce sul funzionamento dell’organismo, dando luogo a una malattia. Queste malattie si possono trasmettere alla prole in vari modi.

RISULTATI
Il 90% dei pazienti che si sottopone a un trattamento di Procreazione Assistita raggiunge la gravidanza.
ASSISTENZA
Il 97% dei nostri pazienti raccomanda IVI.
IVI offre attenzione personalizzata e assistenza in tutte le fasi del trattamento.
TECNOLOGIA
Le cliniche IVI sono pioniere nello sviluppo di tecnologie di Procreazione Assistita di ultima generazione per offrire i migliori risultati.
QUALITÀ/PREZZO
Non siamo l’opzione più cara. Siamo l’opzione che offre più alternative di trattamento per raggiungere i migliori risultati.
Permette di rilevare se ci sono cromosomi in più o in meno negli embrioni, evento conosciuto come alterazione numerica. Ad esempio, la sindrome di Down si manifesta quando, invece di avere due cromosomi del paio 21, ve ne sono tre (trisomia 21). Altre aneuploidie cromosomiche che generano malattie sono trisomia 18, trisomia 13, 45X (Sindrome di Turner), 47XXY (Sindrome di Klinefelter), 47XYY e 47XXX.
Indicazioni:
Il numero di cromosomi di questa cellula (cariotipo) è quello normale, un totale di 46 suddivisi in 23 paia: 22 paia di autosomi e 1 paio di cromosomi sessuali, XX nel caso della donna e XY nell’uomo.
Nonostante questo, il numero di cromosomi di questa cellula è alterato, invece di 46 cromosomi ne esistono 47, perché il paio 21 presenta tre copie, invece di due, evidenziando una sindrome di Down.
Permette di rilevare l’alterazione o mutazione di un gene negli embrioni, causante una malattia monogenica o mendeliana. Questo test analizza diversi tipi di malattie ereditarie –autosomiche recessive, autosomiche dominanti e malattie legate al cromosoma X–, come la fibrosi cistica, la malattia di Huntington, la sindrome dell’X fragile, l’emofilia A, l’anemia falciforme e la malattia di Marfan.
Indicazioni:
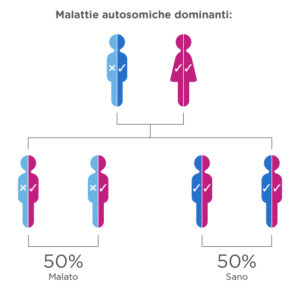
Nel caso delle malattie autosomiche dominanti, uno dei genitori presenta un gene affetto ed è affetto dalla malattia (nell’esempio, l’uomo). La donna non presenta il gene affetto. Della prole, il 50% sarà sano e il 50% avrà il gene mutato, essendo affetto dalla malattia.
Al contrario, nel caso di una malattia autosomica recessiva, il fatto di avere solo una delle due copie del gene non vuol dire che si è affetti dalla malattia, ma solo esserne portatori. Per presentare la malattia, entrambe le copie, materna e paterna, dovrebbero avere il gene mutato. In questo caso, il 25 % della discendenza sarà sana, il 50 % portatore sano e solo il 25 % malato.
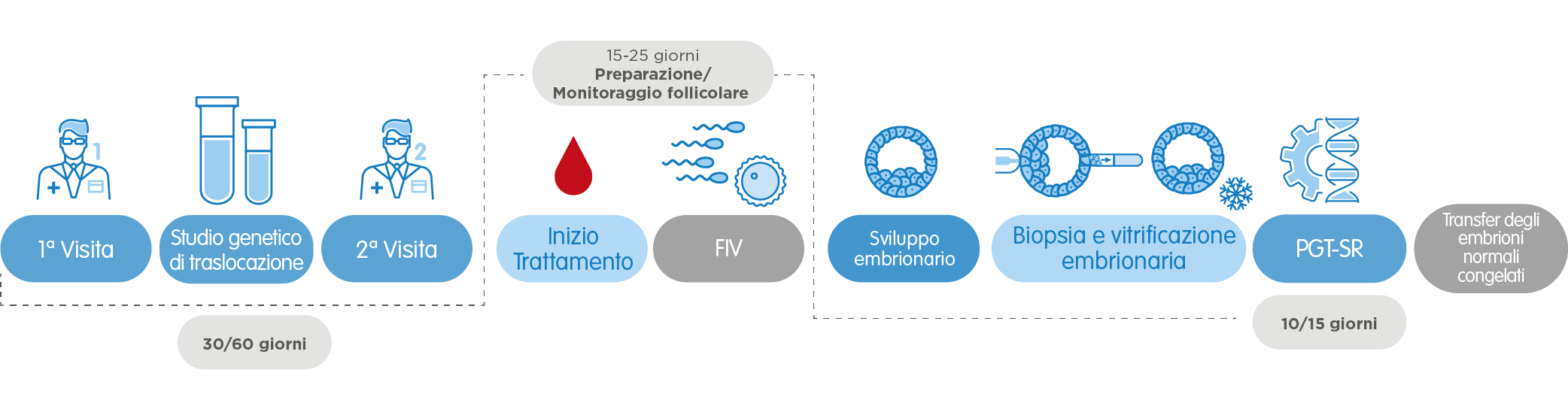
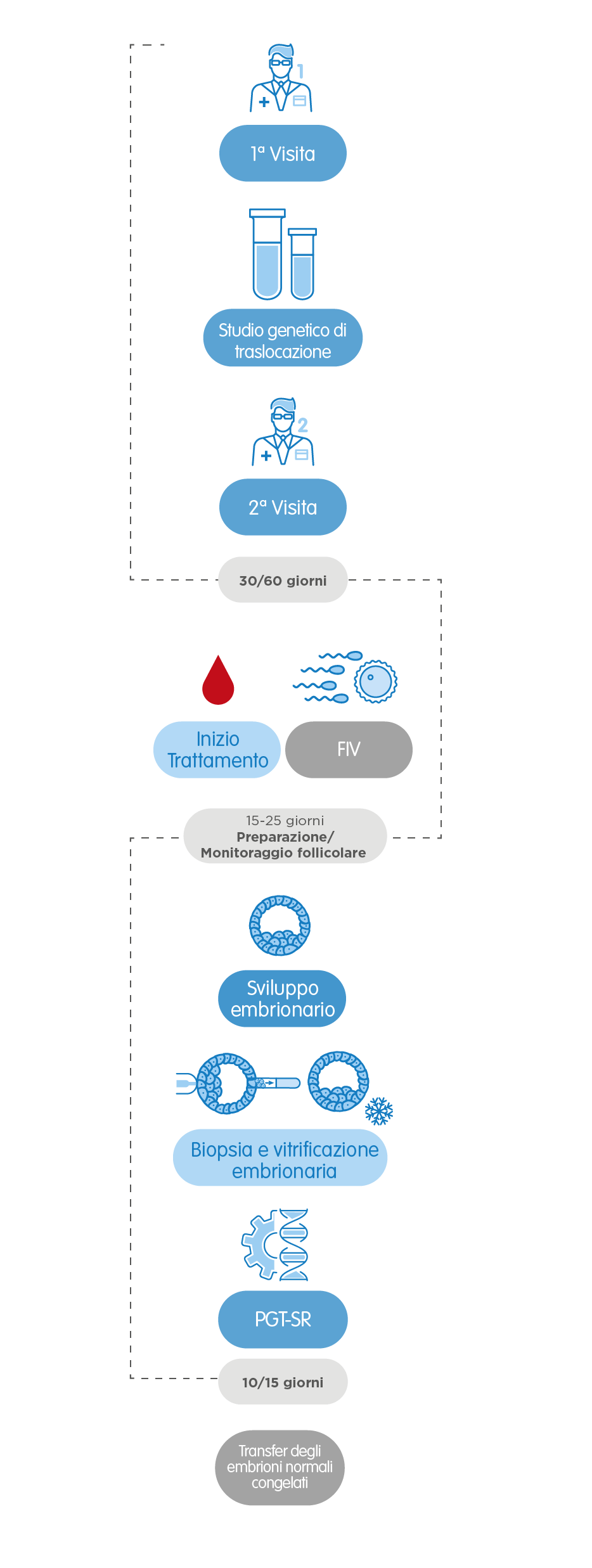
3. PGT-SR, il Test Genetico Preimpianto per la rilevazione di alterazioni strutturali
Permette di rilevare negli embrioni la presenza di cromosomi anomali per la rottura o unione incorretta di vari segmenti. Esistono molti tipi di anomalie cromosomiche strutturali –traslocazioni, delezioni, duplicazioni, inserzioni, ad anello, inversioni – che a volte possono essere compensate (equilibrate) o meno, evento conosciuto come alterazioni in squilibrio. In quei casi in cui, a causa dell’alterazione strutturale del cromosoma, il gene non è corretto, si ha come risultato la malattia.
Indicazioni:
Anomalie cromosomiche strutturali:
Traslocazioni: avvengono quando due frammenti di uno dei cromosomi della coppia si rompono e si scambiano di posizione. In questo caso, il cambio non coinvolge i geni di quel cromosoma, che continuano a funzionare: è un’anomalia equilibrata.
Nel seguente esempio, due frammenti di due cromosomi si rompono e si scambiano di posizione. Avviene una perdita o un guadagno, secondo il caso, dei geni dei cromosomi: è un’anomalia squilibrata.
Nell’ultimo esempio, avviene una fusione di due cromosomi acrocentrici (che presentano solo un braccio) da un’estremità, cosa che aumenta il rischio di trisomia dei cromosomi coinvolti.
Delezioni: una porzione di uno dei cromosomi, nel momento della rottura e del tentativo di ricomporsi, si perde, di conseguenza i geni di quella zona sono modificati.
Duplicazioni: un segmento di un cromosoma si duplica, per cui avviene un guadagno dei geni di quella regione.
Inserzioni: un frammento di un cromosoma si stacca dal luogo di origine e si inserisce in un altro cromosoma.
Cromosomi ad anello: un frammento di uno dei cromosomi della coppia si rompe alle estremità e cerca di ripararsi unendo i frammenti fra loro, formando un anello; in questa riparazione si lasciano fuori due porzioni, che si perdono. I geni che si trovavano in quel cromosoma non possono continuare a funzionare con normalità, per cui generano una malattia.
Inversioni: in una porzione di uno dei cromosomi, si verificano due rotture, una porzione gira e si unisce di nuovo all’altra. A seconda del tipo di unione, questa rottura si può riparare in modo equilibrato o no.
Ogni tipo di PGT ha le sue particolarità, ma in tutti è necessario realizzare un ciclo di Fecondazione in Vitro per poter analizzare geneticamente gli embrioni risultanti.
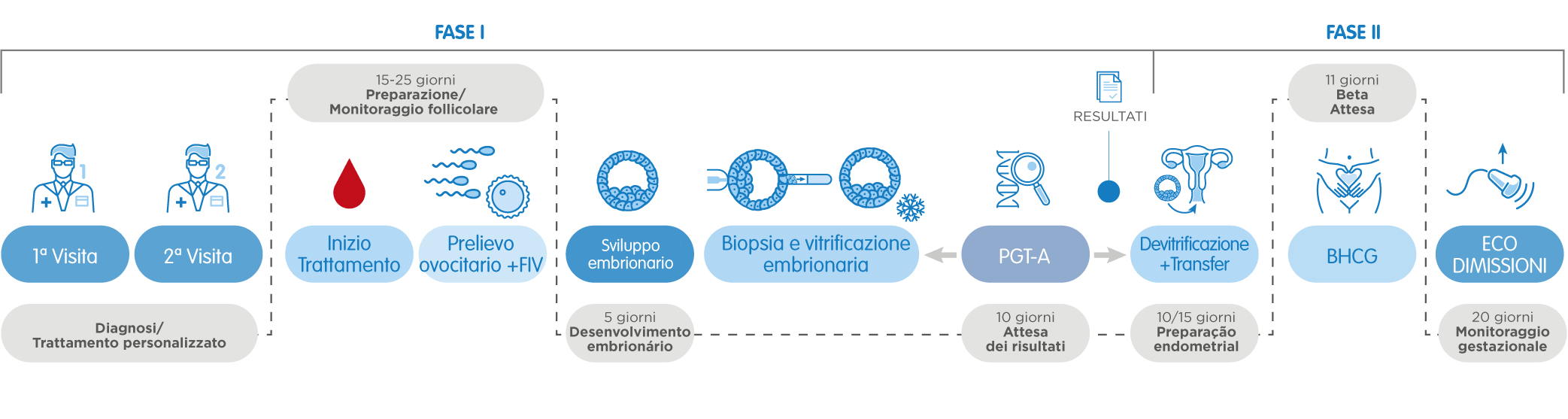
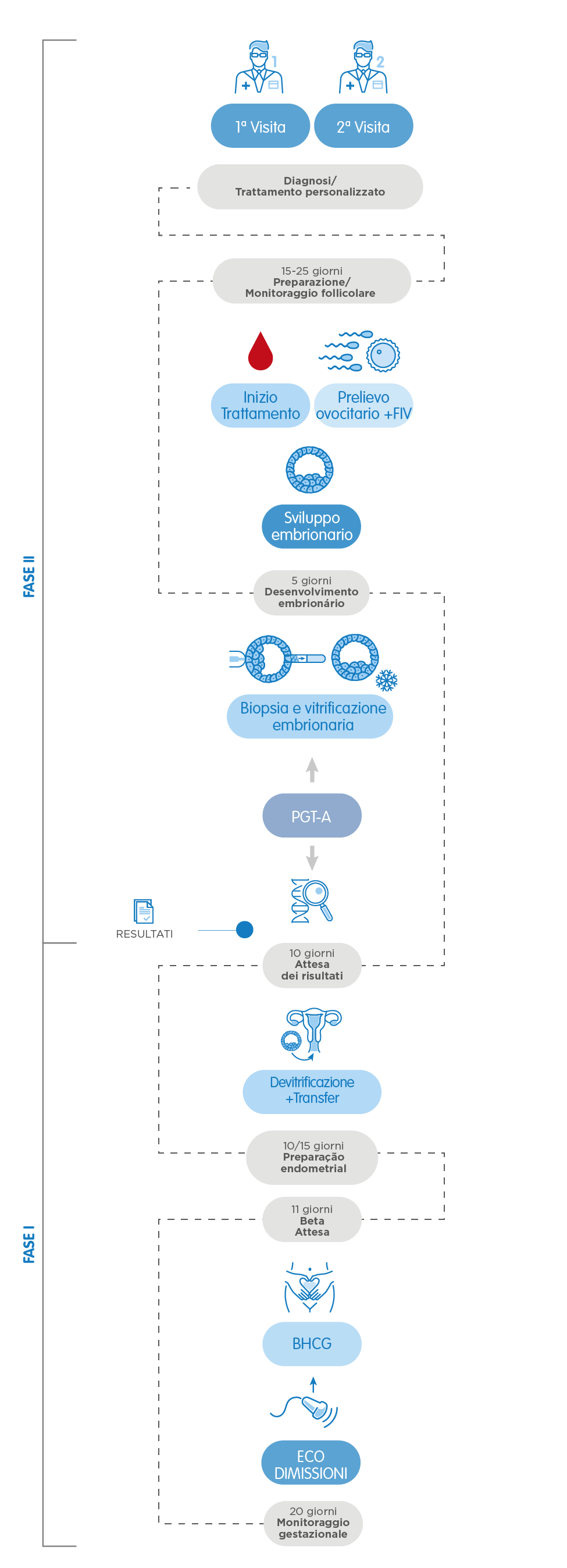
Così, dopo la prima visita con il ginecologo, il trattamento inizia in base alla mestruazione. Dopo 10-14 giorni di stimolazione ovarica controllata, si procede all’ottenimento degli ovuli (pick-up ovarico). Una volta fecondati con il seme di donatore o del partner, se il caso, gli embrioni si lasciano in coltura fino alla fase di blastocisti, che corrisponde alla quinta o sesta giornata dopo il pick-up.
In questa fase, si estrae un piccolo numero di cellule di ogni embrione – tecnica nota come biopsia embrionaria – e si procede all’analisi genetica. Lo stesso giorno, si congelano (vitrificano) gli embrioni biopsiati in attesa del risultato dell’analisi genetica.
La data del risultato varia a seconda del tipo di test effettuato: 10 giorni per il PGT-A, 10-15 giorni per il PGT-SR e il PGT-M. Una volta ottenuto il risultato, si prepara l’endometrio della paziente per il transfer. Ottenuti embrioni sani adatti al transfer (cioè normali cromosomicamente e/o in cui non è presente la malattia genetica analizzata), si procede alla devitrificazione di uno di essi e al transfer nell’utero materno. Il resto degli embrioni rimane congelato per eventuali usi futuri.
Nel caso particolare del PGT-SR, per rilevare alterazioni strutturali, può essere necessario uno studio previo di traslocazione, che tarda dai 30 ai 60 giorni a seconda del tipo di alterazione cromosomica. Il resto del processo è simile.
Per ultimo, nel caso del PGT-M per la rilevazione di malattie monogeniche, è necessario uno studio previo di informatività che fornisce informazioni su come procedere in ogni caso concreto. La durata di questa fase varia secondo il tipo di gene alterato, e può variare da 6 settimane a 4 mesi. Esiste la possibilità che sia necessario elaborare un protocollo specifico per la malattia che si vuole rilevare e che il procedimento si allunghi fino a 3 mesi aggiuntivi. In ogni caso, i pazienti saranno guidati in ogni momento dai nostri specialisti per realizzare il procedimento in totale serenità, fiducia e con monitoraggi personalizzati.
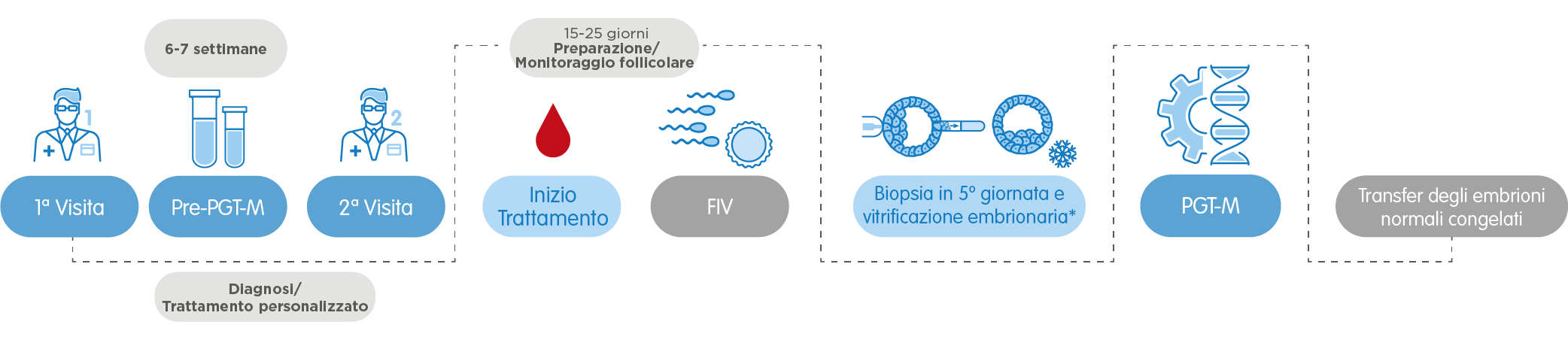
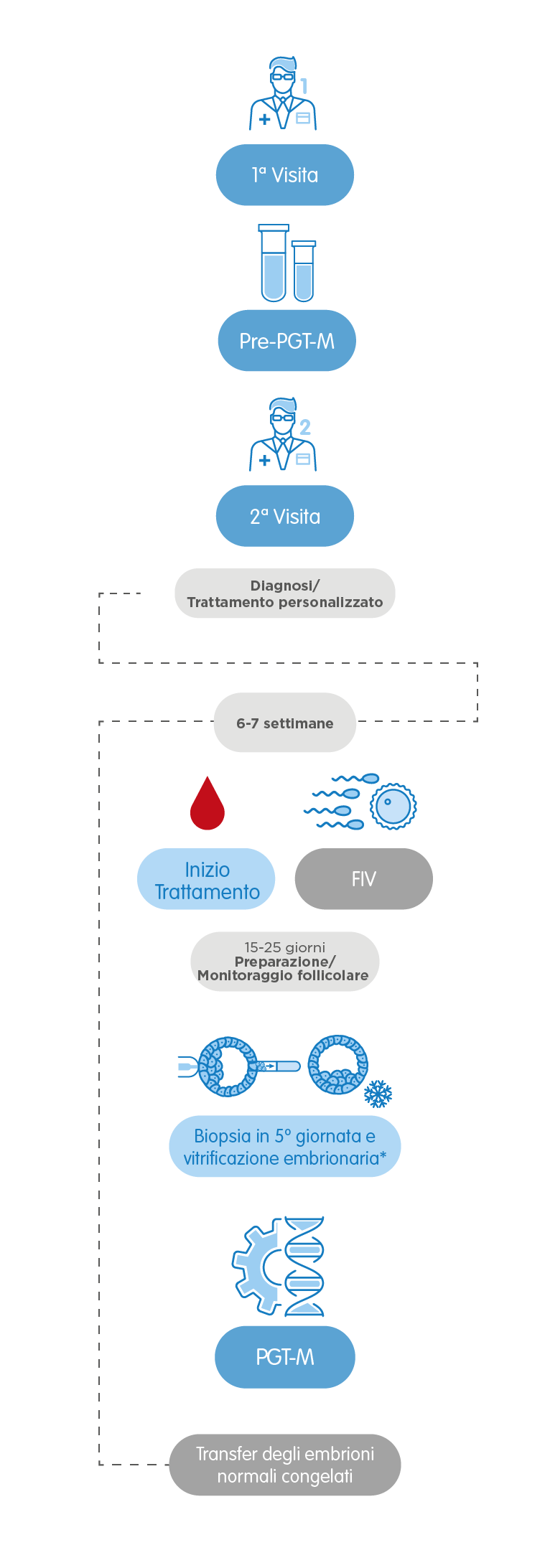
Ogni tipologia di PGT ha le sue caratterestiche, per poter procedere all’analisi genetica degli embrioni è sempre necessario realizzare un ciclo di fecondazione in vitro. Dopo 13-15 giorni di stimolazione ovarica, si ottengono gli ovociti che verranno fecondati con il seme del donatore o del partner. Gli embrioni vengono quindi coltivati fino allo stadio di blastocisti, circa 5-6 giorni dopo il prelievo. Successivamente si esegue la biopsia embrionale e si attendono circa 10-15 giorni per l’arrivo dei risultati con l’esito della diagnosi preimpianto. Dopo la preparazione dell’endometrio, in un ciclo successivo, verranno trasferiti gli embrioni considerati ottimali per generare una gravidanza.